首页 > 答疑解惑 > 实验室常见问题
发布时间:2023-11-30 浏览量:456 下载
实验室应对非标准方法、实验室开发的方法、超出预定范围使用的标准方法、或其他修改的标准方法进行确认。
一、方法确认的意义
方法确认(method validation)指实验室通过试验,提供客观、有效的证据以证明特定方法满足预期的用途。方法确认应当建立方法的性能特性和使用的限制条件、识别影响方法性能的因素及影响程度、确定方法所适用的基体以及方法的正确度和精密度。
实验室在使用非标准方法前应进行确认,以确保该方法适用于预期的用途,并提供相关证明材料。确认应尽可能全面,以满足预期用途或应用领域的需要。
二、需要确认的方法
需要确认的非标准方法包括实验室开发的方法、超出预定范围使用的标准方法、其他修改的标准方法等。
三、方法确认的时机
当实验室使用非标准方法、实验室开发的方法、超出预定范围使用的标准方法或其他修改的标准方法时,应首先进行确认。当修改已确认过的方法时,应确定这些修改的影响;当发现影响原有的确认时,应重新进行方法确认。
当实验室开发方法时,可按照以下步骤进行相应的方法确认。
实验室开发的方法指由实验室自己为检测或校准活动制定的非标准方法。实验室可能由于新产品(材料)没有现成可使用的方法、或出自研究与分析的目的、或为节省时间和降低成本、或国际贸易的需要而制定检测和校准方法。
CNAS-CL01认可准则中7.2.1.6条款规定,当需要开发方法时,应予以策划,并指定具备能力的人员,并为其配备足够的资源。在方法开发的过程中,应进行定期评审,以确定持续满足客户需求。开发计划的任何变更应得到批准和授权。因此,实验室需要开发方法时,应至少确保做到以下4个方面:
(1)开发的策划。实验室为其自身目的而开发检测/校准/抽样新方法是一个设计过程,因此需要进行策划与控制。在进行新方法开发策划时,实验室应确定:
①设计和开发的阶段,制定阶段计划;
②适合于每个开发和设计阶段的评审、验证和确认活动;
③设计开发的职责、权限和接口。
实验室应将新方法的开发作为一个项目来进行管理。实验室应对参与设计和开发的不同小组之间、不同部门之间和不同单位之间的接口(包括组织接口和技术接口)进行管理,以确保相互间有效的沟通,并明确职责分工。
随着设计开发的进展,在适当时,策划的输出(如计划)应予以更新,并确保所有有关人员之间的有效沟通。新方法的开发应交给经授权且有能力的人员进行,实验室管理者应保障其有足够的资源(人力资源、物质资源及信息资源)。
(2)开发的评审。评审是为确定主题事项达到规定目标的适宜性、充分性所进行的活动。评审的目的是确保设计结果满足要求的能力。在适宜的阶段,实验室应依据策划的安排对新方法的设计开发工作进行系统的评审,识别存在的问题并提出必要的改进措施,以确保设计开发的结果满足输入要求。评审的内容可以包括:
①输出的结果及对应的内、外部资源;
②满足设计输入要求的适宜性和充分性;
③设定目标达到的程度;
④识别存在的问题,提出纠正措施。
评审的参加者应包括与所评审的设计开发阶段有关的职能代表,评审的方式可以采用会议评审、文件评审或聘请专家评审等。实验室应记录评审结果及任何必要的改进措施。
(3)变更的控制。实验室应识别新开发的方法的变更,任何变更应得到批准和授权,并保持有关记录。也就是说,适当时,应对开发的变更进行评审、验证和确认,并在实施变更前得到批准和授权。对方法开发的变更应包括评审变更对数据和结果以及已交付数据和结果的影响。变更的评审结果及任何必要的改进措施的记录应予以保持。
(4)开发的确认。为确保数据和结果能满足规定的使用要求或已知的预期用途的要求,实验室应依据所策划的安排对设计开发进行方法确认。
四、确定方法性能特性的技术
(1)方法的性能特性
当按预期用途评估被确认方法的性能特性时,实验室应确保满足客户的需求并符合规定的要求。方法性能特性可包括但不限于:测量范围、准确度、结果的测量不确定度、检出限、定量限、方法的选择性、线性、重复性或复现性、抵御外部影响的稳健度或抵御来自样品或测试物基体干扰的交互灵敏度以及偏倚。典型的化学分析方法确认参数的选择参见下表。
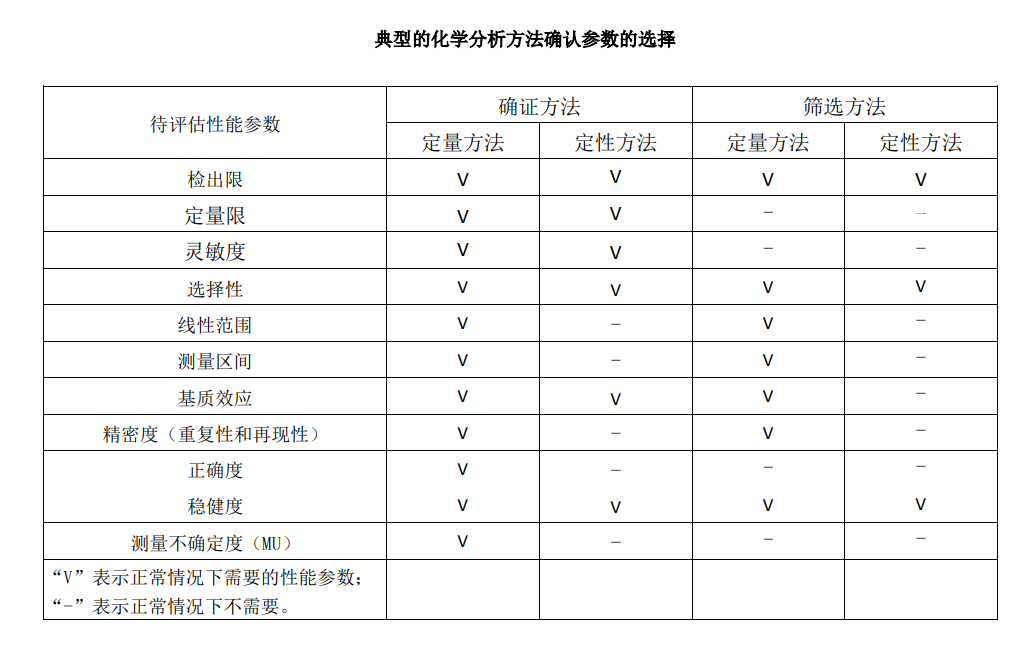
(2)用于方法确认的技术
方法的确认既可在实验室内部进行,也可将方法确认委托给外部机构进行。如果由外部机构实施方法确认,实验室应最终决定方法的适宜性,并在使用前进行方法验证。对方法的预期用途进行评价时,由经过确认的方法所得数据的范围和准确度应满足客户需要。确认可能包括样品的抽取、处置和传送程序。
不同技术领域的确认要求有显著的差异。一般地说,确认的深入程度和广泛程度应与方法预期的用途相符。方法确认是在成本、风险和技术可行性之间进行平衡的结果。实验室应根据方法的理论基础、技术要求、客户要求、业务风险等因素进行综合考虑,确定方法确认的程序和具体要求。可用以下一种或多种技术进行方法确认:
①使用参考标准或标准物质进行校准或评估偏倚和精密度;
②对影响结果的因素进行系统性评审;
③通过改变受控参数来控制检验方法的稳健度,如培养箱温度、加样体积等;
④与其他已确认的方法进行结果比对;
⑤实验室间比对;
⑥根据对方法原理的理解和抽样或检测方法的实践经验,评定结果的测量不确定度。
实验室如果缺乏选择合适的确认技术的经验的话,可以针对所需要确认的方法的需求,参考国际或区域专业组织或实验室认可机构已经发布的方法确认指南类文件进行。例如:
ASTM D 6708 测量同种物质相同特性两种检测方法间预期协议的统计评定和改进的标准操作
ASTM D 7235 建立在线分析与基准检测方法结果之间线性相关关系
GB/T 27417-2017 合格评定化学分析方法确认和验证指南
GB/T 32465-2015 化学分析方法验证确认和内部质量控制要求
SN/T 3223-2012 动物传染病PCR检测技术确认规范
SN/T 3224-2012 动物传染病ELISA检测技术确认规范
SN/T 3266-2012食品微生物检验方法确认技术规范
SN/T 4561-2016转基因检测非标方法确认评价指南
NY/T 2887-2016 农药产品质量分析方法确认指南
随着经济全球化和“一带一路”倡议的推进,很多政府、组织或贸易双方越来越重视和要求方法的等效性。所谓“方法等效性评估”指评定替代方法和参考方法的检测结果有无显著性差异的程序,即通过使用两种方法检测同一样品,对所得结果进行统计学分析,并与方案中预设的可接受限进行比较,如果没有显著性差异则认为两种方法是等效的,否则认为不等效。“等效性评估”是方法“确认”的一种主要形式,通过与参考方法的比较获得替代方法的性能特性,进而做出其是否能够满足特定目的用途的判定。国内已有规范性文件发布,例如:
GB 18510-2001 煤和焦炭试验可替代方法确认准则
SN/T 2775-2011商品化食品检测试剂盒评价方法
WS/T 420-2013 临床实验室对商品定量试剂盒分析性能的验证
五、方法确认的记录
实验室应保存以下方法确认记录:
(1)使用的确认程序;
(2)规定的要求;
(3)确定的方法性能特性;
(4)获得的结果;
(5)方法有效性声明,并详述与预期用途的适宜性。